说到杀死癌细胞,两种药物往往比一种好。一些药物组合提供了一个组合拳,更有效地杀死细胞,需要更低剂量的每种药物,并可以帮助防止耐药性。
麻省理工学院的生物学家现在发现,通过结合现有的两种药物,这两种药物都针对癌细胞的分裂能力,可以显著提高药物的杀伤能力。研究人员说,这种药物组合似乎也能在很大程度上使正常细胞存活,因为癌细胞的分裂方式与健康细胞不同。他们希望在一到两年内开始这种组合的临床试验。
“这是很多人已经在使用的一类药物与多家公司正在开发的另一类药物的组合,”戴维h科赫(David H. Koch)科学教授、麻省理工学院精确癌症医学中心(MIT Center for Precision Cancer Medicine)主任迈克尔亚菲(Michael Yaffe)说。“我认为这为在患者中快速翻译这些发现开辟了可能。”
这一发现是由研究人员开发的一个新软件程序实现的,该程序揭示了其中一种药物具有一种此前未知的作用机制,可以极大地增强另一种药物的效果。
亚菲同时也是科赫综合癌症研究所的成员,他是这项发表在7月10日出版的《细胞系统》杂志上的研究的资深作者。科赫研究所的科学家杰西·帕特森和布莱恩·乔因是这篇论文的第一作者。
意想不到的协同作用
亚菲的实验室长期以来一直对分析癌细胞中活跃的细胞通路很感兴趣,目的是找出这些通路如何在信号网络中协同工作,从而制造出可被多种药物靶向的疾病特异性弱点。当研究人员开始这项研究时,他们正在寻找一种药物,可以增强PLK1抑制剂的作用。一些干扰细胞分裂的PLK1抑制剂已经被开发出来,其中一些正在进行2期临床试验。
基于他们之前的工作,研究人员知道PLK1抑制剂也会产生一种叫做氧化的DNA和蛋白质损伤。他们假设,将PLK1抑制剂与一种阻止细胞修复氧化损伤的药物配对,可能会使它们发挥更好的作用。
为了探索这种可能性,研究人员测试了一种PLK1抑制剂和一种名为TH588的药物,它可以阻止MTH1,一种帮助细胞对抗氧化损伤的酶。这种结合对许多类型的人类癌细胞非常有效。在某些情况下,研究人员可以同时使用每一种药物原剂量的十分之一,并达到与单独使用这两种药物相同的细胞死亡率。
“这真的很惊人,”Joughin说。“这比你通常从合理设计的组合中看到的协同作用更强。”
然而,他们很快意识到这种协同作用与氧化损伤无关。当研究人员对缺失MTH1基因的癌细胞进行治疗时,他们发现这种药物组合仍然以同样高的速度杀死癌细胞。他们认为MTH1基因是TH588的目标基因。
“然后我们真的陷入了困境,因为我们有一个很好的组合,但我们不知道为什么它会起作用,”亚菲说。
为了解开这个谜团,他们开发了一个新的软件程序,可以让他们识别出受药物影响最严重的细胞网络。研究人员测试了29种不同类型的人类癌细胞的药物组合,然后将数据输入软件,软件将结果与这些细胞系的基因表达数据进行比较。这使得他们能够发现与两种药物之间的高或低协同水平相关的基因表达模式。
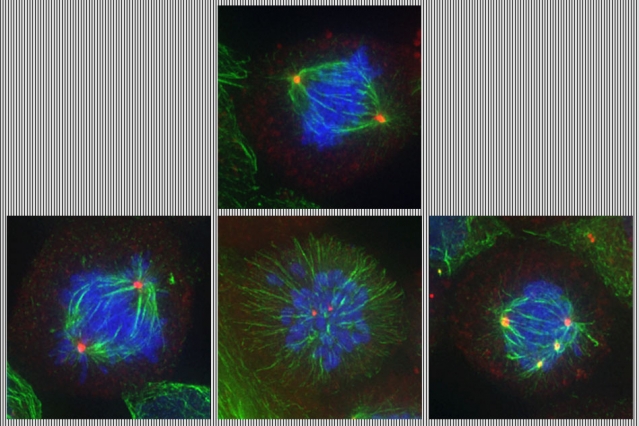
这项分析表明,这两种药物都是针对有丝分裂纺锤体的。有丝分裂纺锤体是在细胞准备分裂时染色体排列在细胞中心时形成的结构。实验室的实验证实了这是正确的。研究人员已经知道PLK1抑制剂针对有丝分裂纺锤体,但他们惊讶地发现TH588也影响了相同的结构。
“我们发现的这种组合非常不明显,”亚菲说。“我从来没有给过两种药物,它们都针对同样的过程,而且预期的效果比单纯的相加效果更好。”
“这是一篇令人兴奋的论文,原因有两个,”达纳-法伯/哈佛癌症中心(Dana-Farber/Harvard Cancer Center)基础科学副主任戴维•佩尔曼(David Pellman)表示。首先,Yaffe和他的同事在合理设计药物治疗组合方面取得了重要进展。其次,如果你喜欢科学之谜,这是一个引人入胜的分子侦查例子。一种曾被认为以某种方式起作用的药物被揭开了神秘面纱,通过一种完全不同的机制发挥作用。”
干扰有丝分裂
研究人员发现,虽然他们测试的两种药物都破坏有丝分裂,但它们似乎以不同的方式破坏有丝分裂。TH588与微管结合,微管形成有丝分裂纺锤体,减缓其组装。许多类似的微管抑制剂已经用于临床治疗癌症。研究人员表示,其中一些微管抑制剂也能与PLK1抑制剂协同作用,他们认为,与他们最初测试的药物TH588相比,这些微管抑制剂可能更容易用于患者的快速使用。
虽然PLK1蛋白参与细胞分裂和纺锤体形成的多个方面,但目前还不清楚PLK1抑制剂是如何干扰有丝分裂纺锤体产生这种协同作用的。亚菲说,他怀疑它们可能阻断了染色体沿着纺锤体运动所必需的一种运动蛋白。
这种药物组合的一个潜在好处是,协同效应似乎专门针对癌细胞分裂,而不是正常细胞分裂。研究人员认为,这可能是因为癌细胞在细胞分裂时被迫依赖其他策略,因为它们的染色体往往过多或过少,这种状态被称为非整倍体。
帕特森说:“基于我们所做的工作,我们提出,这种药物组合针对的是癌细胞分裂方式的一些根本不同之处,比如细胞分裂检查点的改变、染色体数目和结构的改变,或者癌细胞的其他结构差异。”
研究人员目前正致力于识别生物标志物,以帮助他们预测哪些患者对这种药物组合反应最佳。他们还试图确定负责这种协同作用的PLK1的确切功能,希望找到其他药物来阻止这种相互作用。
这项研究是由美国国立卫生研究院资助,查尔斯和马约莉Holloway基金会卵巢癌研究基金,麻省理工学院精密癌症医学中心,科赫研究所达纳法伯/哈佛大学癌症中心桥项目,美国癌症协会博士后奖学金(核心)的科赫研究所支持格兰特从美国国家癌症研究所和环境健康中心的支持。
新闻旨在传播有益信息,英文原版地址:http://news.mit.edu/2019/cancer-mitosis-drugs-combine-0710