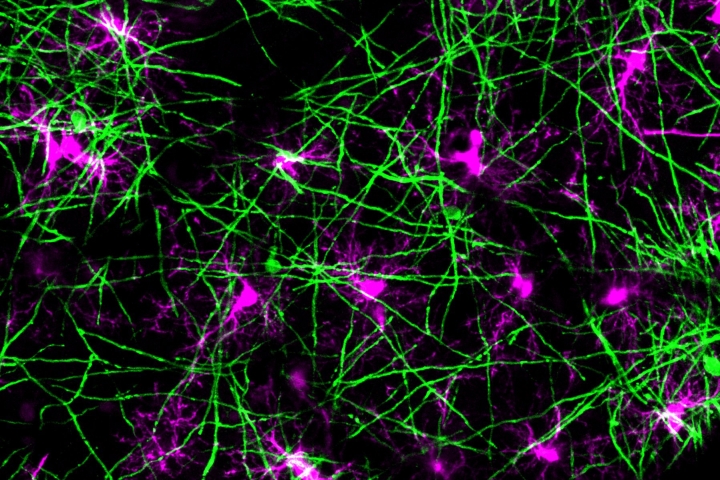
对于少突胶质细胞(对大脑功能至关重要的中枢神经系统细胞)来说,年龄可能不会带来智慧,但它确实具有比科学家所知道的更长的时间来维持生命的力量。这是根据3月27日《神经科学杂志》(Journal of Neuroscience)封面上的一项新研究得出的。
达特茅斯学院的研究人员报告说,成熟的少突胶质细胞在致命的创伤后花了令人震惊的45天才死亡,该创伤在预期的24小时内杀死了年轻的细胞。研究结果表明,有一种新的途径可以逆转或预防衰老和多发性硬化症等疾病对这些重要细胞造成的损害。
在大脑中,少突胶质细胞包裹在称为轴突的神经细胞之间的长而细的连接周围,在那里它们产生一种称为髓鞘的脂质膜,覆盖在轴突上。轴突传递神经细胞用来交流的电信号;髓鞘(如铜线上的塑料涂层)有助于这些信号更有效地传输。
老年和神经退行性疾病(如多发性硬化症)会损害少突胶质细胞。当细胞死亡时,它们的髓鞘生成会随之消亡,导致髓鞘分解,没有任何东西可以补充它们。这可能导致运动功能、感觉和记忆的丧失,因为神经元失去了沟通的能力。
我们认为这向我们展示了随着年龄的增长,大脑中会发生什么,并揭示了这些细胞在老年人中是如何死亡的。这种独特的机制对于我们进一步调查很重要。
科学家们认为,受损的少突胶质细胞(如所有受伤的细胞)会启动一种称为细胞凋亡的细胞自毁,其中细胞会自我杀死。但达特茅斯学院的研究人员发现,成熟的少突胶质细胞在死亡前可以经历前所未有的延长寿命。这些发现提出了一个关键问题,即这些细胞在成熟时会发生哪些变化,从而使它们能够持续存在。
“我们发现成熟细胞的途径仍然受到控制,但不是经典的程序性细胞死亡途径,”生物科学助理教授、该论文的通讯作者罗伯特希尔说。
“我们认为这向我们展示了随着年龄的增长,大脑中会发生什么,并揭示了这些细胞如何在老年人中死亡,”希尔说。“这种独特的机制对于我们进一步调查很重要。我们需要了解为什么这些细胞遵循这种途径,以便我们可以根据疾病背景潜在地鼓励或预防它。
第一作者Timothy Chapman,Guarini ’23,作为Hill研究小组的博士候选人领导了该项目,他说,开发保存髓鞘的治疗方法的努力集中在培养年轻的少突胶质细胞和保护成熟的少突胶质细胞上。但这项研究表明,随着年龄的增长,细胞可能会发生显着变化,一刀切的治疗方法可能不起作用。
“为了回应同样的事情,年轻细胞会走一条路,而老细胞会走另一条路,”查普曼说,他现在是斯坦福大学的博士后研究员。“如果你想保护老细胞,你可能不得不做一些与帮助年轻细胞成熟完全不同的事情。你可能需要一种双重方法。
该论文建立在该团队于 2023 年 3 月在《自然神经科学》杂志上报道的活组织模型之上,该模型允许他们启动单个少突胶质细胞的死亡,以观察其周围的细胞如何反应。他们报告说,当年轻大脑中的少突胶质细胞死亡时,它周围的细胞会立即补充丢失的髓鞘。然而,在相当于60岁老人的大脑中,周围的细胞什么也没做,髓鞘也丢失了。
“这个模型让我们尽可能接近大脑中发生的细胞死亡过程,”希尔说。“我们能够很好地模拟衰老的影响。我们能够选择单个少突胶质细胞,观察它死亡,观察它再生或无法再生,这使我们能够了解是什么在细胞水平上驱动了这一过程以及如何控制它。
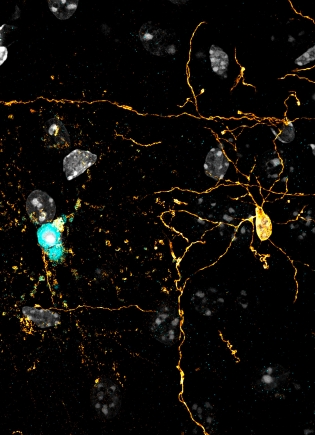
在最新的研究中,研究人员使用他们的模型致命地破坏了少突胶质细胞DNA,这相当于细胞死亡射线 – 希尔开发的一种名为2Phatal的基于光子的设备。他们还使用了去除髓磷脂的标准方法,该方法使用铜基毒素铜利酮作为比较。
正如先前的研究报道的那样,未成熟的细胞很快死亡。但是较老的细胞继续存在,达特茅斯研究小组最初将其解释为对DNA损伤的抵抗力。
当研究人员在45天后使用希尔实验室开发的长期高分辨率成像技术检查成熟细胞时,这项研究成为焦点。“那时我们看到,并不是细胞对损伤有抵抗力 – 它们正在经历这种延长的细胞死亡,”希尔说。
“从来没有人检查过DNA损伤后这么长时间的细胞死亡。这是我们在文献中可以找到的唯一一个例子,一个细胞经历了这样的创伤性事件,并且停留时间超过一周,“他说。
查普曼说,因为人类终生都有少突胶质细胞,所以已知这些细胞会积累DNA损伤,并且比其他细胞更有弹性。“这就是为什么我们认为这种效果适用于衰老。这些细胞可能持续这么长时间的一个原因是因为它们习惯于在衰老中自然地经历这种损伤,“他说。
希尔和查普曼说,这项研究打开了一扇巨大的迷宫的第一扇门,里面有更多问题,比如延长死亡是否是一件好事。它可能相当于功能失调的髓鞘,这比根本没有髓鞘更糟糕,希尔说。它将细胞与周围组织隔离开来,基本上使它缺乏营养。
“这几乎就像有垃圾在轴突上坐了45天。我们是想保存这些垃圾还是加快清除速度?在我们看到这个之前,我们甚至不知道这是一个问题,“希尔说。
“如果我们了解细胞死亡机制,也许我们可以加快速度并摆脱功能失调的髓鞘,”他说。“我们一直在努力拯救细胞和组织,但你必须知道它们是否值得拯救。
新闻旨在传播有益信息,英文版原文来自https://home.dartmouth.edu/news/2024/03/older-brain-cells-linger-unexpectedly-their-death?page=992