
Jeffrey 和 Delinda Johnson 在威斯康星大学麦迪逊校区的实验室工作。 摄影:Sally Griffith-Oh/威斯康星大学麦迪逊分校
一种新开发的模仿蛋白质行为的纳米材料可能是治疗阿尔茨海默氏症和其他神经退行性疾病的有效工具。纳米材料改变了脑细胞中两种关键蛋白质之间的相互作用,具有潜在的强大治疗效果。
最近发表在《先进材料》杂志上的创新发现得益于威斯康星大学麦迪逊分校科学家和西北大学纳米材料工程师之间的合作。
这项工作的重点是改变两种蛋白质之间的相互作用,这两种蛋白质被认为参与了阿尔茨海默氏症、帕金森氏症和肌萎缩侧索硬化症(ALS)等疾病的奠定基础。
第一种蛋白质称为Nrf2,这是一种称为转录因子的特殊类型的蛋白质,可在细胞内打开和关闭基因。
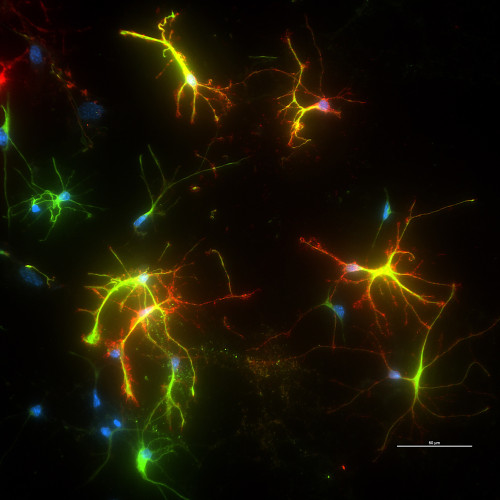
这张图片显示了蛋白质样聚合物(红色)在小鼠模型的脑细胞中的作用。纳米级聚合物旨在改变两种蛋白质之间的相互作用,以对抗细胞中的氧化应激。 图片由约翰逊实验室/威斯康星大学麦迪逊分校提供
Nrf2 的重要功能之一是其抗氧化作用。虽然不同的神经退行性疾病是由不同的疾病过程引起的,但它们之间的共同点是氧化应激对神经元和其他神经细胞的毒性作用。Nrf2 对抗脑细胞中的这种毒性应激,有助于避免疾病。
威斯康星大学麦迪逊药学院教授杰弗里·约翰逊(Jeffrey Johnson)几十年来一直与他的妻子、药学院高级科学家德琳达·约翰逊(Delinda Johnson)一起研究Nrf2作为治疗神经退行性疾病的有希望的靶点。2022 年,Johnsons 和另一组合作者发现,增加大脑中特定细胞类型(星形胶质细胞)的 Nrf2 活性有助于保护阿尔茨海默病小鼠模型中的神经元,从而显着减少记忆丧失。
虽然之前的研究表明,增加Nrf2的活性可以构成阿尔茨海默氏症治疗的基础,但科学家们发现,有效地靶向大脑内的蛋白质具有挑战性。
“很难让药物进入大脑,但也很难找到激活Nrf2的药物,而不会产生很多脱靶效应,”Jeffrey Johnson说。
进入新的纳米材料。这种合成材料被称为蛋白质样聚合物(PLP),旨在与蛋白质结合,就好像它本身就是蛋白质一样。这个纳米级的模仿者是由西北大学化学教授、该大学国际纳米技术研究所教员Nathan Gianneschi领导的团队的产物。
Gianneschi 设计了多种 PLP 来靶向各种蛋白质。这种特殊的 PLP 的结构是为了改变 Nrf2 和另一种称为 Keap1 的蛋白质之间的相互作用。蛋白质的相互作用或途径是治疗许多疾病的众所周知的靶标,因为 Keap1 基本上控制着 Nrf2 何时对氧化应激做出反应并与之抗争。在无压力条件下结合在一起,Keap1 释放 Nrf2 以在需要时完成其抗氧化工作。
Gianneschi和Johnson夫妇通过CHDI基金会的首席科学官Robert Pacifici联系在一起,该基金会资助旨在治疗亨廷顿病(另一种神经退行性疾病)的研究。该基金会过去曾资助过约翰逊和吉安内斯基的工作。
“顺便说一句,Nathan和他在Grove Biopharma的同事,这是一家专注于蛋白质-蛋白质相互作用治疗靶向的临床前生物技术初创公司,他们告诉Robert,他们正在考虑转向靶向Nrf2,”Johnson说。“罗伯特说,’如果你要这样做,你应该打电话给杰夫约翰逊。
很快,Johnson夫妇和Gianneschi正在讨论威斯康星大学麦迪逊分校实验室提供测试Gianneschi的蛋白质样纳米材料所需的小鼠模型脑细胞的可能性。
杰弗里·约翰逊(Jeffrey Johnson)说,他最初对PLP方法持怀疑态度,因为他不熟悉它,而且精确靶向脑细胞中的蛋白质普遍困难。
“但后来内森的一个学生带着它来到这里,把它放在我们的细胞上,如果它效果不好,我会被诅咒的,”他说。“我们当时真的深入研究了它。”
由此产生的研究表明,Gianneschi 的 PLP 在与 Keap1 结合时非常有效,Keap1 释放了 Nrf2 以积累在细胞核中,增强了其抗氧化功能。重要的是,它没有引起不必要的脱靶效应,这些效应阻碍了旨在更好地激活Nrf2的其他策略。
虽然这项工作是在培养的细胞中进行的,但Johnsons和Gianneschi现在在神经退行性疾病的小鼠模型中更进一步。这是他们没想到会参与的一系列研究,但现在很高兴能继续从事。
“我们没有生物材料方面的专业知识,”Delinda Johnson说。“因此,从西北大学获得这一点,然后在威斯康星大学的生物方面向前推进,这表明这些类型的合作非常重要。
新闻旨在传播有益信息,英文版原文来自https://news.wisc.edu/nanomaterial-that-mimics-proteins-could-be-basis-for-new-neurodegenerative-disease-treatments/